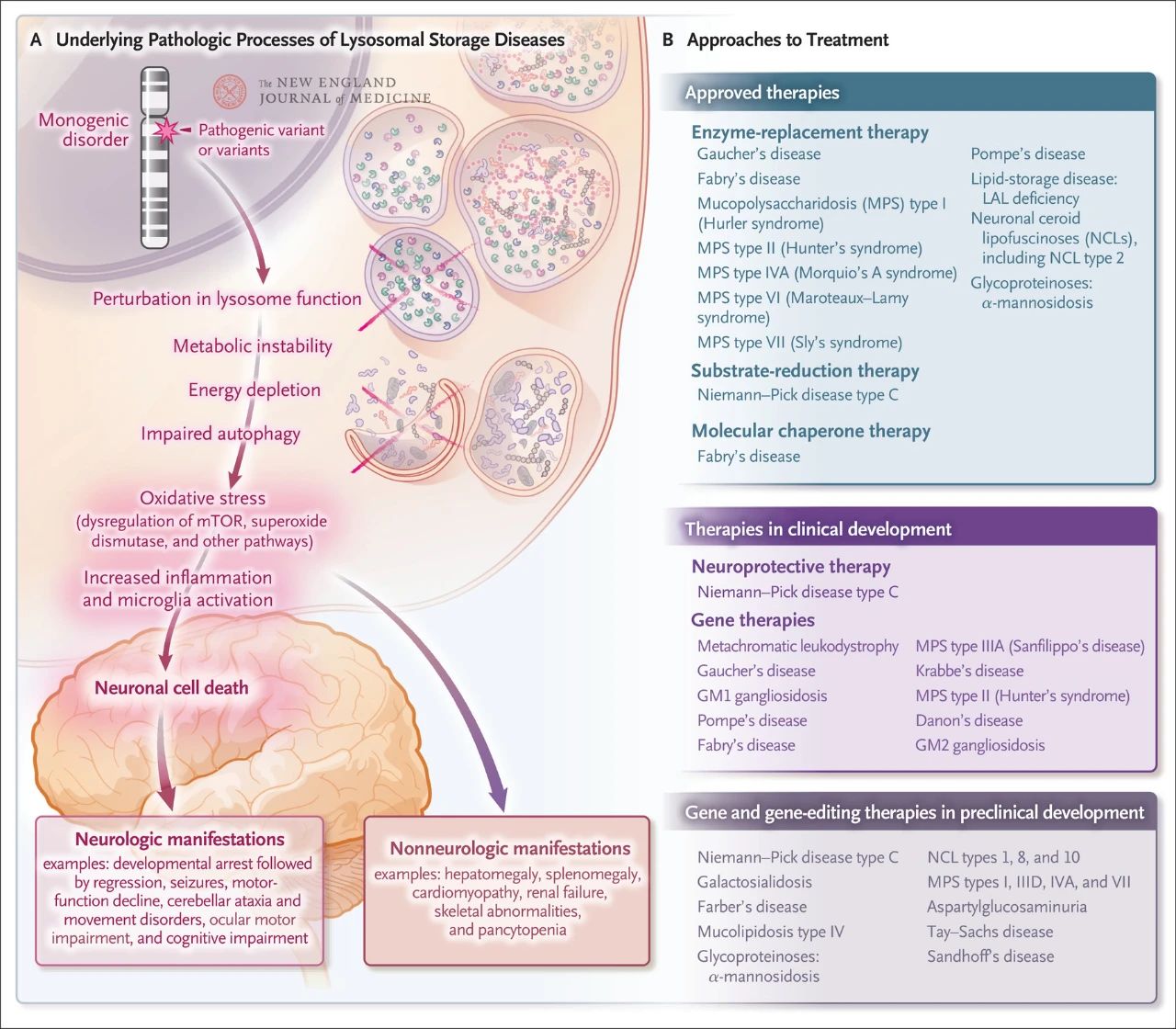
Vaikka lysosomaalinen kertymäsairaus on suhteellisen harvinainen, sen kokonaisesiintyvyys on noin yksi 5 000 elävänä syntynyttä lasta kohden. Lisäksi lähes 70 tunnetusta lysosomaalisesta kertymäsairaudesta 70 % vaikuttaa keskushermostoon. Nämä yhden geenin sairaudet aiheuttavat lysosomaalista toimintahäiriötä, mikä johtaa aineenvaihdunnan epävakauteen, nisäkkäiden kohdeproteiinin rapamysiinin (mTOR, joka normaalisti estää tulehdusta) säätelyn häiriintymiseen, autofagian heikkenemiseen ja hermosolujen kuolemaan. Useita hoitoja, jotka kohdistuvat lysosomaalisen kertymäsairauden taustalla oleviin patologisiin mekanismeihin, on hyväksytty tai on kehitteillä, mukaan lukien entsyymikorvaushoito, substraattien pelkistyshoito, molekyylishaperonihoito, geeniterapia, geenien muokkaus ja hermoja suojaava hoito.
Niemann-pick-taudin tyyppi C on lysosomaalinen varastoituneiden solujen kolesterolikuljetushäiriö, jonka aiheuttavat joko NPC1- (95 %) tai NPC2-geenin (5 %) kaksialleeliset mutaatiot. Niemann-Pickin taudin tyypin C oireisiin kuuluu nopea ja kuolemaan johtava neurologinen heikkeneminen imeväisillä, kun taas myöhäisillä juveniileillä, juveniileilla ja aikuisilla puhkeavilla muodoilla on splenomegalia, supranukleaarinen katsehalvaus ja pikkuaivoataksia, dysartikulaatio ja etenevä dementia.
Tässä lehden numerossa Bremova-Ertl ym. raportoivat kaksoissokkoutetun, lumekontrolloidun, vaihtovuoroisen tutkimuksen tulokset. Tutkimuksessa käytettiin potentiaalista hermosoluja suojaavaa ainetta, aminohappoanalogia N-asetyyli-L-leusiinia (NALL), Niemann-Pickin taudin tyypin C hoitoon. Tutkimukseen rekrytoitiin 60 oireista nuorta ja aikuista potilasta, ja tulokset osoittivat merkittävää paranemista ataksian arviointi- ja arviointiasteikon kokonaispistemäärässä (ensisijainen päätetapahtuma).
N-asetyyli-DL-leusiinin (Tanganil), NALL:n ja n-asetyyli-D-leusiinin raseemisen yhdisteen, kliiniset tutkimukset näyttävät perustuvan pitkälti kokemukseen: vaikutusmekanismia ei ole selvitetty selvästi. N-asetyyli-dl-leusiini on hyväksytty akuutin huimauksen hoitoon 1950-luvulta lähtien; Eläinmallit viittaavat siihen, että lääke toimii tasapainottamalla mediaalisten vestibulaaristen hermosolujen ylipolarisaatiota ja depolarisaatiota. Myöhemmin Strupp ym. raportoivat lyhytaikaisen tutkimuksen tulokset, joissa he havaitsivat oireiden paranemista 13 potilaalla, joilla oli eri syistä johtuva degeneratiivinen pikkuaivoataksia. Nämä löydökset herättivät uudelleen kiinnostuksen lääkkeen uudelleentutkimukseen.
Mekanismi, jolla n-asetyyli-DL-leusiini parantaa hermojen toimintaa, ei ole vielä selvä, mutta kahdessa hiirimallissa tehdyt löydökset, joista toinen tutkii Niemann-Pickin tautia tyyppiä C ja toinen GM2-gangliosidien kertymishäiriön varianttia O (Sandhoffin tauti), joka on toinen neurodegeneratiivinen lysosomaalinen sairaus, tehdyt havainnot ovat herättäneet huomion NALL:ssa. Tarkemmin sanottuna n-asetyyli-DL-leusiinilla tai NALL:lla (L-enantiomeerit) käsiteltyjen Npc1-/- -hiirten eloonjääminen parani, kun taas n-asetyyli-D-leusiinilla (D-enantiomeerit) käsiteltyjen hiirten eloonjääminen ei parantunut, mikä viittaa siihen, että NALL on lääkkeen aktiivinen muoto. Samankaltaisessa GM2-gangliosidien kertymishäiriön varianttia O (Hexb-/-) koskevassa tutkimuksessa n-asetyyli-DL-leusiini johti hiirten eliniän vaatimattomaan mutta merkittävään pidentymiseen.
Selvittääkseen n-asetyyli-DL-leusiinin vaikutusmekanismia tutkijat selvittivät leusiinin metaboliareittiä mittaamalla metaboliitteja mutanttieläinten pikkuaivokudoksissa. GM2-gangliosidin kertymishäiriön variantti O -mallissa n-asetyyli-DL-leusiini normalisoi glukoosi- ja glutamaattiaineenvaihduntaa, lisää autofagiaa ja lisää superoksididismutaasin (aktiivinen hapensieppari) tasoja. Niemann-Pickin taudin C-mallissa havaittiin muutoksia glukoosi- ja antioksidanttiaineenvaihdunnassa sekä parannuksia mitokondrioiden energia-aineenvaihdunnassa. Vaikka L-leusiini on voimakas mTOR-aktivaattori, mTOR:n tasossa tai fosforylaatiossa ei havaittu muutoksia n-asetyyli-DL-leusiinilla tai sen enantiomeereillä käsittelyn jälkeen kummassakaan hiirimallissa.
NALL:n neuroprotektiivista vaikutusta on havaittu hiirimallissa, jossa tutkittiin aivokuoren iskujen aiheuttamaa aivovauriota. Näihin vaikutuksiin kuuluvat neuroinflammatoristen merkkiaineiden aleneminen, aivokuoren solukuoleman vähentäminen ja autofagiavirtauksen paraneminen. NALL-hoidon jälkeen vaurioituneiden hiirten motoriset ja kognitiiviset toiminnot palautuivat ja leesion koko pieneni.
Keskushermoston tulehdusvaste on useimpien neurodegeneratiivisten lysosomaalisten kertymäsairauksien tunnusmerkki. Jos neuroinflammaatiota voidaan vähentää NALL-hoidolla, monien, ellei kaikkien, neurodegeneratiivisten lysosomaalisten kertymäsairauksien kliiniset oireet voivat parantua. Kuten tämä tutkimus osoittaa, NALL:n odotetaan myös olevan synergistinen muiden lysosomaalisten kertymäsairauksien hoitojen kanssa.
Monet lysosomaaliset kertymäsairaudet liittyvät myös pikkuaivoataksiaan. Kansainvälisen tutkimuksen mukaan, johon osallistui lapsia ja aikuisia, joilla on GM2-gangliosidien kertymäsairauksia (Tay-Sachsin tauti ja Sandhoffin tauti), ataksia väheni ja hienomotorinen koordinaatio parani NALL-hoidon jälkeen. Laaja, monikeskustutkimus, kaksoissokkoutettu, satunnaistettu, lumekontrolloitu tutkimus osoitti kuitenkin, että n-asetyyli-DL-leusiini ei ollut kliinisesti tehokas potilailla, joilla oli sekamuotoinen (perinnöllinen, ei-periytyvä ja selittämätön) pikkuaivoataksia. Tämä havainto viittaa siihen, että tehoa voidaan havaita vain tutkimuksissa, joihin osallistuu potilaita, joilla on perinnöllinen pikkuaivoataksia, ja että siihen liittyviä vaikutusmekanismeja analysoidaan. Lisäksi, koska NALL vähentää neuroinflammaatiota, joka voi johtaa traumaattiseen aivovaurioon, NALL-tutkimuksia traumaattisen aivovaurion hoidossa voidaan harkita.
Julkaisun aika: 02.03.2024